* Autor de contacto: jesse.fink@ifpr.edu.br
Recibido:
26-08-21
Recibido con revisiones: 14-03-22
Aceptado:
02-04-22

PRODUÇÃO DE MUDAS E DESENVOLVIMENTO DO LÚPULO EM SOLO
COM DIFERENTES VALORES DE pH e DOSES DE POTÁSSIO
Jessé Fink 1* ; Gustavo Frosi 2, Kayn Bastiani 3, Dayana Eckert 2, Frank Lagos 3,
Ricardo Aparecido Pereira 4, Maurício Martignoni 3
1 Laboratório de Solos, Instituto Federal do Paraná. Palmas, Paraná, Brasil.
2 Departamento de Solos, Universidade Federal do Rio Grande do Sul. Porto Alegre, Rio Grande do Sul, Brasil.
3 Instituto Federal do Paraná. Palmas, Paraná, Brasil.
4 Laboratório de Desenvolvimento de Bebidas, Instituto Federal do Paraná. Palmas, Paraná, Brasil
RESUMO
O lúpulo (Humulus lupulus) é uma planta com potencial de cultivo na região Centro-Sul do Paraná, Brasil. Todavia, não há recomendações brasileiras oficiais quanto à produção de mudas ou à adubação e calagem. O objetivo do trabalho foi avaliar a produção de mudas de lúpulo e verificar o desenvolvimento de plantas de lúpulo crescidas em solo com diferentes valores de pH e doses de K2O, na região Centro Sul do Paraná, Brasil. Três experimentos foram conduzidos: i) estacas de uma planta-matriz foram mergulhadas em uma solução de ácido indol-3-butírico (AIB) à 1% e alocadas em bandejas com diferentes substratos – verificou-se a brotação e sobrevivência das mudas de lúpulo; ii) mudas de lúpulo foram transplantadas para um solo com diferentes valores de pH (4,5; 5,5; 6,0 e 6,5) – avaliou-se o desenvolvimento e absorção de nutrientes pelas plantas; iii) mudas de lúpulo foram transplantadas para um solo com diferentes doses de K2O adicionadas – verificou-se o desenvolvimento e absorção de K pelas plantas. O substrato para produção de mudas não influenciou na brotação das estacas de lúpulo, porém a presença do AIB diminuiu a brotação e o crescimento até 41 dias. O valor de pH 5,5 no solo propiciou o melhor desenvolvimento do lúpulo por aumentar a produção de massa verde e massa seca em comparação ao pH 4,5. Plantas de lúpulo em solo com pH 6,0 e 6,5 apresentaram menor teor de clorofila, mas mantiveram o mesmo padrão de absorção de nutrientes. A produção de massa seca das plantas de lúpulo e o teor de K na massa seca das raízes aumentaram com as doses K2O adicionadas ao solo. No entanto, o K não foi translocado para a parte aérea das plantas, na fase inicial de desenvolvimento.
Palavras-chave: ácido indol-3-butírico; estaquia; acidez do solo; fertilidade do solo.
PRODUCTION OF SEEDLING AND GROWTH OF HOPS ON SOIL
UNDER DIFFERENT PH VALUES AND POTASSIUM DOSES
ABSTRACT
Hops (Humulus lupulus) is a plant with potential for cultivation in the Center-South region of Paraná, Brazil. However, there are no official Brazilian recommendations for production of seedlings or fertilization and liming. The aims of this work were to evaluate the production of hop seedlings and verify the development of hop plants grown in soil with different pH values and K2O rates, in the Center-South region of Paraná, Brazil. Three experiments were carried out: i) cuttings of a plant were dipped in a 1% indole-3-butyric acid (IBA) solution and placed in different substrates – the sprouting and survival of the hop seedlings was verified; ii) hop seedlings were transplanted to a soil with different pH values (4,5; 5,5; 6,0 and 6,5) – the development and nutrients uptake by the plants was evaluated; iii) hop seedlings were transplanted to a soil with different K2O rates added – the development and K uptake by the plants was assessed. The substrate for seedling production did not influence the sprouting of hop cuttings, but the presence of IBA reduced sprouting and growth up to 41 days. The pH 5,5 value in the soil provided the best hop development by increasing the production of fresh and dry biomass in comparison with pH 4,5. Hop plants in soil with pH 6,0 and 6,5 showed lower chlorophyll content, but maintained the same nutrient uptake. The production of dry biomass of hop plants and the K content of the roots increased with the K2O rates added to the soil, However, K was not transferred to the aerial part of the plants in the initial phase of development.
Keywords: indole-3-butyric acid; cuttings; soil acidity; soil fertility.
INTRODUÇÃO
O lúpulo (Humulus lupulus L.) é uma planta perene, trepadeira, oriunda de regiões temperadas da América do Norte, Europa e Ásia e utilizada principalmente na produção de cerveja. O Brasil é o terceiro maior produtor de cerveja no mundo, com uma produção de 140 milhões de hectolitros, ficando atrás apenas da China (460 milhões de hectolitros) e dos Estados Unidos da América (221 milhões de hectolitros). Grande parte do lúpulo utilizado na produção brasileira é importado dos Estados Unidos da América, Alemanha, República Checa e a China (Rodrigues et al., 2015). Estes países atingiram uma produção de 117633 toneladas em uma área plantada de 60544 ha (International Hop Growers’ Convention, 2018). O lúpulo age como conservante natural e confere aroma e sabor à cerveja (Marcos et al., 2011; Peragine, 2011; Ribeiro de Oliveira et al., 2016; Sousa, 2005). O aroma produzido na cerveja está relacionado com o conteúdo de óleos essenciais presentes nas flores femininas do lúpulo, enquanto o sabor amargo está atrelado ao teor α-ácidos (Rosa e Afonso, 2015; Sawicka, 2021).
O Brasil não possui plantações de lúpulo em grande escala, pois são poucos os locais favoráveis ao seu cultivo. Locais entre as latitudes 35° a 55° nos Hemisférios Sul e Norte são os mais adequados para o cultivo (De Oliveira et al., 2019), principalmente porque o lúpulo exige temperaturas médias iguais ou menores que 19.5 °C, além do somatório de excesso hídrico igual ou menor que 100 mm (Thomé et al.,1999). Em adição, a propagação e condução das plantas, tanto do ponto de vista fitotécnico quanto da fertilidade do solo, pode interferir no crescimento e desenvolvimento da cultura e nos teores de óleos essenciais e de α-ácidos que a planta produz.
A propagação do lúpulo pode ser feita através de reprodução vegetativa, o que consiste em originar plantas idênticas à matriz. A estaquia é o principal meio de reprodução da cultura, o qual é um processo simples e prático, pois de apenas um ramo é possível produzir uma grande quantidade de mudas (Sposito et al., 2019). O enraizamento destas estacas depende de inúmeros fatores, como a idade da planta e nutrição mineral da planta matriz, luminosidade, temperatura, umidade e reguladores de crescimento. Os principais reguladores vegetais relacionados com o processo de reprodução vegetal por estaquia são das famílias das auxinas e das citocininas. As auxinas, como o ácido indol-butírico (AIB), são reguladores vegetais capazes de induzir a formação e alongamento de hastes e caules no nível da planta, além de induzir a produção de diferentes raízes adventícias nos tecidos de folhas e caules recém retirados da planta mãe e formação de dominância apical (Alcantara-Cortez et al., 2019; Macháčková et al., 2008). Porém, o substrato no qual a estaca será inserida também deverá possuir características que promovam a aeração e disponibilidade de água e nutrientes de acordo com a exigência da planta (Cunha et al., 2006).
O lúpulo é uma cultura bastante exigente em fertilidade do solo. Segundo a recomendação de fertilizantes oficial do Reino Unido (Department for Environment, Food and Rural Affairs [DEFRA], 2010), a cultura se desenvolve adequadamente em pH 6,3-6,5, com teores de P disponível (método Olsen) acima de 41 mg kg-1 e K e Mg disponível (extração por nitrato de amônio) acima de 241 e 51 mg L-1, respectivamente. Estes valores podem ter magnitudes diferentes nos solos de altitude do Sul do Brasil, uma vez que o poder tampão nutricional e de acidez são diferentes dos solos europeus. Assim, a calibração da acidez e da disponibilidade de nutrientes para o cultivo do lúpulo pode ser uma chave para iniciar o desenvolvimento do cultivo desta planta que é altamente rentável.
Este trabalho teve o objetivo de: a) avaliara produção de mudas de lúpulo em diferentes substratos, com e sem aplicação de ácido indol-3-butírico; e b) verificar o desenvolvimento e a absorção de nutrientes pelas plantas de lúpulo crescidas em solo com diferentes valores de pH; e c) o desenvolvimento inicial da cultura com doses crescentes de potássio em um Latossolo da região Centro Sul do Paraná, Brasil.
MATERIAL E MÉTODOS
Descrição do local
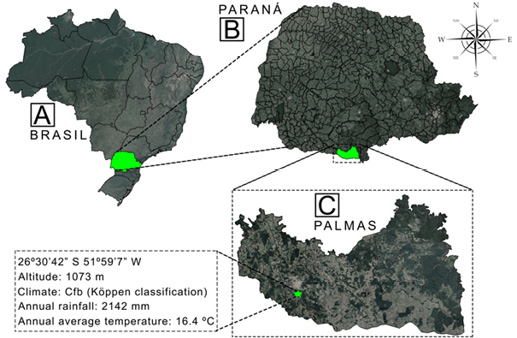
O experimento foi desenvolvido em Palmas, na região Centro Sul do Paraná, Brasil (Figura 1). O município está sob influência do clima Cfb (classificação de Köppen - clima temperado com verão ameno [mês mais frio acima de 0 ºC e todos os meses com média abaixo de 22 °C]). As temperaturas máximas e mínimas anuais variam entre 22 e 23°C e 12 e 13°C, respectivamente, e a precipitação pluviométrica anual é de 2142 mm (Instituto agronômico do Paraná [IAPAR], 2020). A área experimental fica localizada à 1073 m de altitude (Figura 1).
Figura 1. Localização do município de Palmas (C) no Estado do Paraná (B) e no Brasil (A) e características climáticas da área experimental.
Figure 1. Location of Palmas county (C) in Paraná State (B) and in Brazil (A) and climatic characteristics of the experimental area.
Três experimentos foram conduzidos: a) produção de mudas de lúpulo em laboratório; b) desenvolvimento de lúpulo à campo em solo com diferentes valores de pH; e c) desenvolvimento inicial de mudas de lúpulo sob diferentes doses de potássio (K). Os experimentos foram conduzidos paralelamente, pois a ideia do primeiro experimento surgiu no decorrer da tentativa de produção de mudas de lúpulo para o segundo e terceiro experimento.
Experimento A: produção de mudas de lúpulo
A produção de mudas de lúpulo foi realizada pelo método de estacas oriundas de uma planta matriz. Foram produzidas 45 estacas que mediam de 10 a 12 cm e continham uma única folha. As estacas foram submetidas à dois tratamentos (2 fatores), imediatamente após sua produção. O primeiro fator experimental foi: a) 30 estacas foram mergulhadas em solução de 1% de ácido indol-3-butírico por 10 segundos (Com AIB); e b) 15 estacas não tiveram contato com o AIB (Sem AIB). Essas estacas foram acomodadas em bandejas que continham 5 tipos de substratos (segundo fator experimental): a) substrato de casca de pinus triturada (CP); b) substrato comercial (SC); c) 60% turfa + 40% vermiculita (TV); d) 60% turfa + 20% vermiculita + 20% areia (TVA); e) turfa 60% + 40% cinza (TC). Assim, para cada substrato havia 6 repetições para as estacas com AIB e três repetições para as estacas sem AIB.
As estacas foram plantadas no dia 20/12/2018 e mantidas em sala com luminosidade controlada (12h de luz). Nos dias 28/01/2019 e 29/03/2019 (40 e 100 dias após o transplante [40 DAT e 100 DAT, respectivamente]), o número de brotos e sua altura foram avaliados. Ainda, 100 DAT mediu-se o índice SPAD relativo à clorofila A e total, com um clorofilômetro marca Falker (FalkerChlorophyll Index - clorofiLOGFalker).
Experimento B: desenvolvimento de lúpulo em solo com diferentes valores de pH
A avaliação do desenvolvimento do lúpulo em função pH do solo se deu por meio de covas. Cavou-se 32 covas de 96 dm3 (40 cm de comprimento x 40 cm de largura x 60 cm de profundidade) em um Latossolo (Empresa Brasileira de Pesquisa Agropecuária [Embrapa], 2018) e Oxisol no Soil Taxonomy (SoilSurvey Staff, 2014). O solo retirado dessas covas foi homogeneizado e logo após coletou-se uma amostra para caracterização química, a qual indicou: pH= 4,5; Ca = 0,2 cmolc dm-3; Mg = 0,7 cmolc dm-3; Al = 1,0 cmolc dm-3; H+Al = 7,7 cmolc dm-3; K= 51 mg dm-3; P= 1,3 mg dm-3; matéria orgânica = 25,5 g dm-3; saturação por bases = 13%; e saturação por alumínio = 49%.
Os valores de pH foram ajustados para 4,5 (pH natural); 5,5; 6,0 e 6,5 com doses de 0, 178, 293 e 413 g dm-3 de calcário filler, que correspondem a 0; 3; 7; 6; 1 e 8,6 Mg ha-1, respectivamente (Comissao de Química e Fertilidade do Solo para os estados do Rio Grande do Sul e de Santa Catarina [CQFS-RS/SC], 2016). As doses de calcário foram aplicadas no início de outubro de 2018. Para isso, o corretivo foi homogeneizado na massa de solo correspondente a cada cova com auxílio de uma betoneira e, logo após, foi acomodado nas covas, totalizando 8 repetições por tratamento.
Como não existe recomendação oficial para o lúpulo no Brasil, o fertilizante fosfatado e potássico adicionado ao solo foi a dose necessária para aumentar os teores de P e K ao nível crítico (CQFS-RS/SC, 2016), mais a dose recomendada para a manutenção da cultura de acordo com a recomendação de adubação para o lúpulo do Reino Unido (DEFRA, 2010). Assim, no dia 26 de outubro de 2018, 44 g de superfosfato simples, 11g de cloreto de potássio e 11 g de ureia, correspondendo a 500 kg P2O5 ha-1, 400 kg K2O ha-1 e 300 kg N ha-1, respectivamente, foram incorporadas manualmente na camada 0-20 cm do solo. Ainda, 15 e 30 dias após o transplante, mais 11 g de ureia foram aplicados por cova.
Em cada cova foi instalado uma estaca, na qual possuía um fio de sisal que se estendia até um cabo a 7 m de altura. Esta estrutura foi montada de forma que as plantas recebessem insolação na maior parte do dia. As mudas de lúpulo foram transplantadas no dia 28 de outubro de 2018, com aproximadamente 15 cm de altura. As plantas foram manejadas de forma a permitir o crescimento de apenas dois ramos, que foram conduzidos no fio de sisal.
Nos dias 20 de dezembro de 2018 e 28 de janeiro de 2019 (54 DAT e 92 DAT) mediu-se a altura das plantas e o índice SPAD relativo à clorofila A, B e total, com um clorofilômetro marca Falker (Falker Chlorophyll Index - clorofiLOGFalker). Em 29 de março de 2019, verificou-se clorose nas folhas, que indicava o início da senescência da cultura. Nesse momento a planta foi cortada ao nível do solo e 10 folhas do terço médio foram coletadas. A massa verde da parte aérea foi pesada e, em seguida, permaneceu por 72 h à 60 ºC em estufa de circulação de ar forçada para medir a massa seca. As 10 folhas coletadas separadamente foram secas nas condições descritas acima e moídas em um moinho Willey. Em seguida, procedeu-se a extração de elementos com solução HCl 1 mol L-1, em banho-maria a 80°C (Silva et al., 2009). A solução foi passada em papel filtro. No extrato filtrado foram determinados os teores de Ca e Mg (espectrometria de absorção atômica), K (fotometria de chama), N (destilação seguida por titulação) e P (espectrometria de absorção molecular).
Experimento C: desenvolvimento inicial de lúpulo sob diferentes doses de K
O experimento para avaliar o desenvolvimento inicial de plantas de lúpulo com diferentes níveis de adubação potássica foi realizado com solo coletado da 0-20 cm de um Latossolo sob campo nativo. Os teores iniciais de K e P disponíveis eram de 79 e 2,55 mg kg-1, respectivamente, valor de pH de 5,5 e SMP 4,95. O pH do solo foi ajustado, com calcário, para 6,0, uma vez que é o pH indicado para o adequado desenvolvimento da maioria das culturas do Sul do Brasil e com o qual Oliveira (2016) obteve os melhores resultados. Também, realizou-se a adição de fertilizante fosfatado para atingir o nível crítico de disponibilidade do nutriente (CQFS-RS/SC, 2016). Esse solo foi misturado com areia (1:1), buscando uma maior aeração para o melhor desenvolvimento das mudas de lúpulo. Posteriormente, o solo foi transferido para vasos de 3 L e adicionados cinco doses de adubação potássica: 0, 50, 125, 200 e 300 kg K2O ha-1. Os vasos foram dispostos em um delineamento inteiramente casualizado, com quatro repetições.
As plântulas de lúpulo tinham, em média, 5 cm quando foram transplantadas para os vasos. As plantas se desenvolveram por 37 dias, até serem colhidas. Neste momento, determinou-se a altura das plantas. Após, a massa vegetal foi seca e os teores de teores de P, K e Na da parte aérea e na raiz foram determinados (Silva et al., 2009). Ainda, coletou-se amostras de solos, nas quais verificou-se a disponibilidade P, K e Na, além dos valores de pH e índice SMP (Tedesco et al., 1995).
Analise estatística
Os resultados foram submetidos à ANOVA fatorial para o experimento A (dois fatores: AIB [2 níveis] X substratos [5 níveis]), à ANOVA one-way para o experimento B e C (quatro níveis de pH de solo ou cinco doses de adubação potássica). Quando diferenças significativas foram encontradas (p<0,05), as médias foram comparadas pelo teste Tukey (α = 0,05; experimento A e B) ou por meio de análise de regressão (experimento C - doses de K2O versus teor de K disponível no solo e teor K na massa seca da raiz). Ainda, a taxa de sobrevivência, avaliada no experimento A, foi obtida pela percentagem de estacas que sobreviveram em relação ao total de estacas avaliadas. A análise estatística foi realizada com auxílio do software Statistix v.10.0 (Analytical Software, Tallahassee, Fl, USA).
RESULTADOS E DISCUSSÕES
Experimento A: produção de mudas de lúpulo
Os dados de sobrevivência das estacas de lúpulo não foram submetidas à analise estatística tradicional, mas indicam algumas tendências quanto aos tratamentos aplicados. As estacas que não receberam o tratamento com AIB tiveram uma taxa de sobrevivência de 93%, enquanto as estacas que foram expostas ao AIB, a taxa de sobrevivência foi de apenas 57%. A taxa e sobrevivência em função do substrato foi de 78% para o SC e TC, 67% com o uso de CP e TV e 56% para TVA. A menor taxa de sobrevivência observada nas estacas expostas à ação do AIB poderia ser devido a alta concentração utilizada. Quando em concentrações muito elevadas, as auxinas passam a exercer toxidade as plantas e ocasionam efeito herbicida (HRAC, 2013). A concentração de AIB a ser utilizada depende de algumas variáveis como o tipo e tamanho do material vegetal. Em geral estacas lenhosas e de maior tamanho suportam uma concentração maior da auxina, do que estacas do tipo herbácea e de menor tamanho (Peralta et al., 2017; Souza et al., 2018). No entanto, o fator determinante da concentração é a espécie da planta (De Alvarenga e Carvalho, 1983). Baixas concentrações de 1500 e 2000 mg L-1 reduziram o percentual de plantas com brotação nas espécies de Passiflora caeruleae Morus sp, respectivamente (De Medeiros et al., 2017; Mayer et al., 2017). Já em plantas da espécie Vaccinium myrtillus e Sapium glandulatum, o uso de até 8000 mg L-1 não ocasionou danos por toxidade (Ferreira et al., 2009; Peña et al., 2012). Outras espécies mais tolerantes, a concentração pode chegar até 20000 mg L-1 sem qualquer efeito prejudicial (Sánchez et al., 1998).
Aspectos químicos e físicos tais como, a disponibilidade de nutrientes, ausência de elementos tóxicos, densidade, capacidade de aeração e armazenamento de água, são alguns dos principais fatores que interferem na escolha e na qualidade de um substrato. Os substratos SC e TC disponibilizam nutrientes fundamentais para o desenvolvimento inicial das estacas. Os demais substratos têm menor de nutrientes ou mesmo inertes como a casca de pinus (CP), a vermiculita (TV) e a areia (TVA). Embora em muitas espécies não seja necessário o fornecimento de nutrientes durante a propagação, existem plantas em que a adição de nutrientes na fase inicial é benéfica. Gomes e Krinski (2018) observaram que o uso de substratos que disponibilizam nutrientes ou a adição externa de fertilizantes resultou em melhoria no índice de sobrevivência das estacas de Piper crassinervium Kunth.
O substrato também influencia na sustentação das estacas, na disponibilidade de água e oxigênio no meio para o enraizamento. A adição de vermiculita nos tratamentos TV e TVA pode ter levado a uma redução na densidade do composto e aumento da retenção de água - vermiculita tem valor de densidade menor e maior retenção de água, quando comparada ao SC e TC (Pêgo et al., 2019). Normalmente, substratos de baixa densidade não são capazes de suportar o crescimento de plantas, por outro lado densidades elevadas ocasionam efeito inverso e retardam e dificultam o desenvolvimento radicular (Dos Santos, 2006; Pagliarini et al., 2015). Fagherazzi et al. (2018) testaram diferentes relações de substratos compostos por turfa e casca de arroz no enraizamento de estacas herbáceas das cultivares de lúpulo Columbus e Yakima Gold. Os autores verificaram que a mescla entre os materiais é benéfica, pois, altera a relação entre os macroporos e microporos possibilitando drenagem suficiente para que ocorra trocas gasosas ao mesmo tempo em que há armazenamento e fornecimento de água.
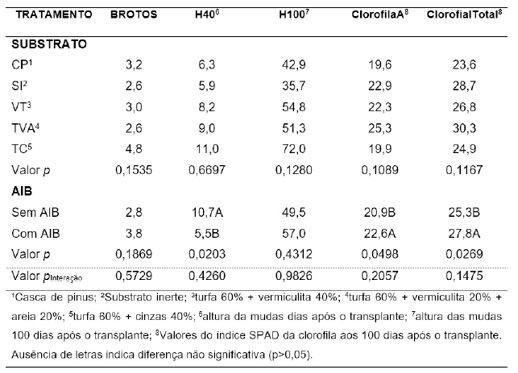
Para as estacas sobreviventes, as variáveis avaliadas não foram influenciadas pela interação dos fatores ou pelo tipo de substrato utilizado (p>0,05; Tabela 1). A altura de planta 40 DAT foi maior nas estacas que não receberam AIB (10,7 cm) do que naquelas que receberam (5,5 cm). Em contrapartida, o índice SPAD relativo à clorofila A e a clorofila total nos 100 DAT foram maiores nas plantas desenvolvidas de estacas tratadas com AIB (p<0,05; Tabela 1). O número de brotos e a altura das plantas 100 DAT não foram influenciadas pelo tratamento com AIB (p>0,05; Tabela 1). A menor altura das plantas que receberam o tratamento com o AIB aos 40 DAT também está relacionada a alta concentração utilizada.
Tabela 1. Características morfológicas de mudas de lúpulo desenvolvidas em diferentes substratos e com adição ou não de ácido indol-3-butírico.
Table 1. Morphological characteristic of hop seedling grown under different substrate and addition or no-addition of indole-3-butyric acid.
Paulus et al. (2020) observaram que plantas de lúpulo tratadas com 1500 mg L-1 de AIB (dose 6 vezes menor que o aplicado neste estudo) apresentaram maior desenvolvimento de parte aérea, comprimento de raiz e número de folhas. Em adição, Machado et al. (2018) observaram que os efeitos positivos do AIB na propagação de lúpulo foram limitados até a concentração de 2800 mg L-1. De Alvarenga e Carvalho (1983) verificaram que há um efeito quadrático do estimulador com auxinas, como o AIB, aplicadas em estacas de frutíferas. A concentração de AIB utilizada em nosso estudo pode ter diminuído o vigor das raízes e repercutido em plantas menores aos 40 DAT (Tabela 1). Oliveira et al. (2009) observaram que o número de raízes aumenta em função da concentrações de AIB, porém, se atinge um máximo e a partir desse a quantidade de raízes começa declinar.
Além de ser importante nos processos de divisão e alongamento celular, as auxinas são antagônicas a fitormônios de senescência. Isso justifica os maiores teores de clorofila (índice SPAD) nas plantas tratadas com AIB. Pois, a auxina pode ter inibido a produção de etileno e retardado a senescência bem como a degradação de moléculas como a da clorofila (Lim et al., 2007; Suttle e Hultstrand, 1991).
Experimento B: desenvolvimento da cultura do lúpulo em solo com diferentes valores de pH
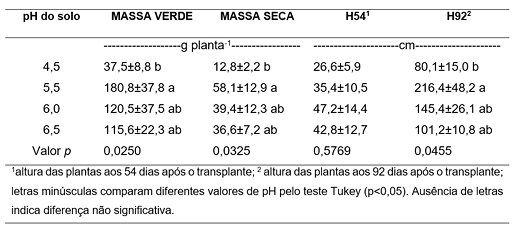
A produção de massa verde, massa seca, altura das plantas 92 DAT (H61) foram maiores para as plantas crescidas em solo com pH 5,5 do que com pH 4,5 (p<0,05; Tabela 2). O pH de 4,5 foi prejudicial à cultura, já que o melhor desenvolvimento do lúpulo ocorre em um pH em torno de 6,5 a 7,0 ( Souza, 2005; Sposito et al., 2019). Valores baixos de pH do solo tendem a influenciar a disponibilidade de nutrientes e o teor de Al3+. De uma maneira geral, à medida que o valor de pH do solo diminui também há uma diminuição na disponibilidade de nutrientes aniônicos (como P, S e N) e aumento no teor de Al3+, o qual influencia negativamente o desenvolvimento das raízes (Barber, 1995; Moraes e Gusmão, 2021) afetando o desenvolvimento da planta. Oliveira et al. (2019) avaliaram o efeito de diferentes valores de pH de um Cambissolo Háplico sobre o desenvolvimento de lúpulo e observaram que a altura de planta foi maior em solos com pH 5,5 do que em solos com pH 5,0, 6,0 ou 6,5, enquanto que a massa seca das plantas não foi influenciada. Entretanto, a cultura tolera uma faixa de pH bastante ampla, podendo estar entre 4,8 e 8,0 (Amoriello, 2019). Possivelmente, este é o motivo que teores de macronutrientes nas folhas de lúpulo apresentaram diferenças não significativas em função dos valores de pH de solo estudado (Tabela 3).
Tabela 2. Massa verde, massa seca e altura das plantas de lúpulo desenvolvidas em solo com diferentes valores de pH.
Table 2. Fresh biomass, dry biomass and height of hop plants grown in soil with different pH values.
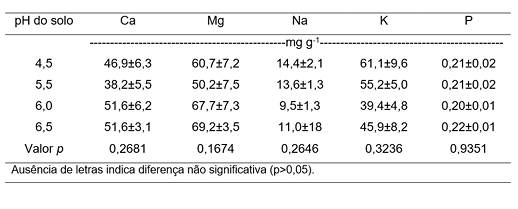
Tabela 3. Teor de nutrientes na folha de plantas de lúpulo desenvolvidas em solo com diferentes valores de pH.
Table 3. Leaf nutrient content of hop plants grown in soil with different pH values.
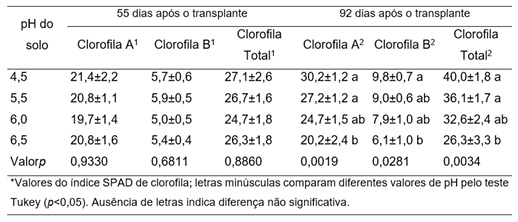
O teor de clorofila das plantas aos 92 DAT também foi influenciado pelo pH do solo (Tabela 4). As plantas cultivadas em solo com valores de pH de 4,5 ou 5,5 apresentaram os maiores índices SPAD. Esta resposta pode estar relacionada como efeito do pH do solo na disponibilidade e dinâmica dos nutrientes – a disponibilidade do Fe é inversamente proporcional ao pH do solo. O Fe não é um constituinte direto da clorofila, entretanto, a protoporfirina, anel orgânico heterocíclico, possui em seu centro um átomo de Fe, denominado grupo heme, a qual é uma precursora da clorofila. O Fe também é necessário para a conversão da protoporfirina em protoclorofilida, molécula intermediária da biossíntese de clorofila (Barker e Pilbeam, 2006; Marschner, 2012; Wang et al., 2017).
Tabela 4. Índice de clorofila (SPAD) de plantas de lúpulo desenvolvidas em solos com diferentes valores de pH.
Table 4. Chlorophyll index (SPAD) of hop plants grown in soil with different pH values.
Experimento C: desenvolvimento inicial da cultura do lúpulo sob diferentes doses de K
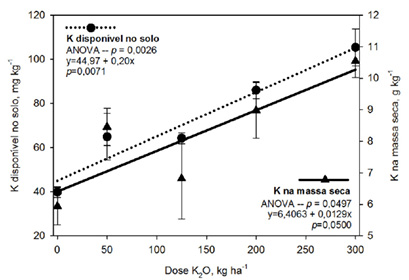
A aplicação de doses de K2O aumentou o teor de K disponível no solo e na massa seca de raiz (p≤0,05; Figura 2). Isso se deve pela aplicação das doses crescentes do fertilizante, que libera uma grande quantidade de K para a solução do solo, o que resulta em uma maior disponibilidade deste nutriente. Com este incremento do nutriente, aumenta a diferença de potencial osmótico entre a solução do solo e a raiz da planta, o que leva a maior absorção do nutriente (Taiz et al., 2017). Além disso, de forma geral, as plantas possuem uma maior demanda por K em sua fase inicial, podendo acumular até 40% de todo o K necessário para o seu desenvolvimento nesta fase (Karlen et al., 1988).
Figura 2. Teor de K disponível no solo e teor K na massa seca das raizes das plantas de lúpulo crescidas sob diferentes doses de K2O.
Figure 2. Available K available in the soil and K content in the roots dry biomass of hop plants grown under different rates of K2O.
Ainda, tanto a maior disponibilidade como o acúmulo de K nas raízes se devem ao pH do solo, que se manteve em um valor médio de 6,4. Os resultados corroboram com o trabalho de Oliveira (2016), que também verificou acúmulo de K na raiz do lúpulo em solo com valor de pH próximo a 6,0. O lúpulo é uma cultura muito exigente em fertilizante potássico e requer o nutriente em nível alto no solo (Marcos et al., 2011). Por outro lado, os teores de Na e P no tecido radicular não variaram em função das doses de K estudadas.
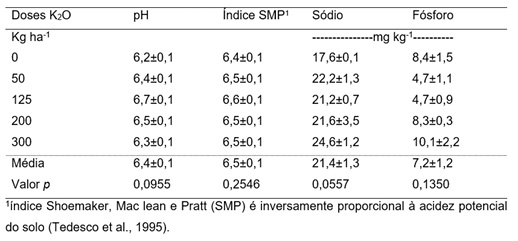
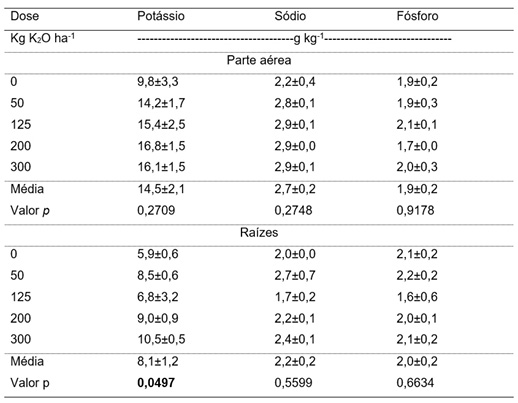
Os valores de pH e o índice SMP do solo não mostraram alterações com as diferentes doses do fertilizante aplicado (Tabela 5). Durante a solubilização do fertilizante potássico, na forma de KCl, não ocorre a liberação de íon H+ ou de hidroxilas, o que não lhe confere poder de alterações no pH do solo. Isso foi observado por Catani e Gallo (1954), em que a aplicação de K, através de KCl, apresentou pouca ou nenhuma influência no pH do solo. Da mesma forma, os teores de P e Na do solo não foram influenciados, já que, todas as unidades experimentais receberam a mesma dose de fertilizante fosfatado e não houve interação com a adubação potássica. As concentrações de macronutrientes na parte aérea da planta não apresentaram diferença em relação as doses de K2O aplicadas (p>0,05; Tabela 6).
Tabela 5. Parâmetros químicos do solo que recebeu diferentes doses de K2O para o cultivo do lúpulo.
Table 5. Chemical parameters of soil that received different rates of K2O for hop cultivation.
Tabela 6. Teor de nutrientes absorvidos e armazenados na parte aérea e raízes de lúpulo.
Table 6. Content of uptake and stored nutrients in hop shoots and roots.
Contudo, trabalhos futuros devem ser conduzidos até o final do ciclo da cultura, a fim de avaliar a fase reprodutiva e a dinâmica do K neste período, já que, normalmente, plantas na fase adulta requerem maiores concentrações de K da solução do solo. Este estudo permitiria avaliar a exigência em fertilização potássica da cultura ao longo do ciclo, tanto para identificar a translocação do K para a parte aérea, como para verificar se a planta apresenta melhoria na sustentação de sua massa vegetal.
CONCLUSÃO
A brotação e a sobrevivência de estacas de lúpulo, aparentemente, são influenciadas pelo tipo de substrato utilizado para a produção, porém o mergulho das estacas em AIB diminui sua brotação. Estudos mais específicos sobre o tema e com avaliações estatísticas poderiam trazer informações mais precisas.
O solo com pH do solo 5,5 permite o melhor crescimento das plantas no primeiro ano de plantio, porém a absorção de nutrientes a planta não é influenciada pelo pH do solo. Em adição, plantas cultivadas em solo com valores de pH de solo 6,0 e 6,5 tendem a diminuir a concentração de clorofila nas folhas.
O aumento da dosagem de K2O aumenta os teores de K no solo, permitindo que a planta de lúpulo absorva e acumule maior quantidade de K nas raízes. Todavia, na fase inicial de desenvolvimento do lúpulo, aparentemente, há pouca translocação de K para a parte aérea da planta.
AGRADECIMENTOS
Este trabalho foi apoiado pelo Instituto Federal do Paraná e Fundação Araucária, por conceder bolsa de iniciação científica (Edital Nº 05/2019 - DIPE/PROEPPI; PIBIS/FA 2017/2017) e auxílio ao pesquisador (Edital Nº 05/2019 - DIPE/PROEPPI).
REFERENCIAS
Amoriello, T. (2019). Multi-Criteria approach for land suitability assessment of hop cultivation in Italy. International Journal of Agriculture and Environmental Research, 2, 277-286.
Barker, A. V. e Pilbeam, D. J. (2006). Handbook of plant nutrition. Taylor & Francis. New York.
Catani, R. A. e Gallo, J. R. (1959). Efeitos determinados no solo pelo uso contínuo de fertilizantes. Bragantia, 13, 75-83.
Comissao de Química e Fertilidade do Solo para os estados do Rio Grande do Sul e de Santa Catarina. (2004). Manual de adubação e calagem para os estados do Rio Grande do Sul e de Santa Catarina. Sociedade Brasileira de Ciência do Solo, Porto Alegre.
Cortes, J. S. A., Jovanna, A. G., David A. C. J. e Melida, S. M. R. (2019). Principales reguladores hormonales y sus interacciones en el crecimiento vegetal. Nova, 17, 109-129.
De Alvarenga, L. R. e Carvalho, V. D. (1983). Uso de substâncias promotoras de enraizamento de estacas frutíferas. Informe Agropecuário, 9, 47-55.
De Medeiros, C. F. M., Pereira, G. A., Mendonça, V., Pereira, E. C., Silva, F. S. O., De Oliveira, L. M. e Cardoso, R. (2017). Tipos de estacas e concentrações de ácido indol-butírico (IBA) na propagação de amora (Morus nigra). Revista Facultad de Agronomía Universidad Nacional de La Plata, 116, 187-191.
De Oliveira, M. V. R. (2016). Crescimento do Lúpulo Influenciado por Calagem e Fornecimento de Fósforo [Dissertação de mestrado]. Universidade do Estado de Santa Catarina.
Dos Santos, F. G. B. (2006). Substratos para Produção de Mudas Utilizando Resíduos Agroindustriais [Dissertação de mestrado]. Universidade Federal Rural de Pernambuco.
Department for Environment, Food and Rural Affairs. (2010). The Stationery Office.
Economic Commission Summary Reports. (2016). International hop growers convention.
Empresa Brasileira de Pesquisa Agropecuária. (2018). Sistema Brasileiro de Classificação de Solo. Sociedade Brasileira de Ciência do Solo.
Fagherazzi, M. M., Santos, M. F., Santos, K. V., Rufalo, L. e Moreira, K. V. (2018). Propagação de estacas de lúpulo sob diferentes substratos. Jornada da Pós-Graduação e Pesquisa-Congrega Urcamp, 15, 1400-1409.
Ferreira, B. G. A., Zuffellato-Ribas, K. C., Carpanezzi, A. A., Tavares, F. R. e Koeshler, H. S. (2009). Metodologias de aplicação de AIB no enraizamento de estacas semilenhosas. Revista Brasileira de Plantas Medicinais, 11(2), 196-201.
Gomes, E. M. e Krinski, D. (2018). Piper crassinervium Kunth vegetative propagation: influence of substrates and stem cuttings positions. Pesquisa Aplicada & Agrotecnologia, 11, 51–59.
HRAC. (2013). Classification of Herbicides according to site of action. http://www.weedscience.org/Documents/ShowDocuments.aspx?DocumentID=1193
Instituto agronômico do Paraná. (2019). http://www.iapar.br.
Macháčková, I., Zažímalová, E. e George, E.F. (2008). Plant Growth Regulators I: Introduction; Auxins, their Analogues and Inhibitors. In: Plant Propagation by Tissue Culture 3rd Edition. Dordrecht.
Karlen, D. L., Flannery, R. L. e Sadler, E. J. (1988). Aerial Accumulation and partitioning of nutrients by corn. Agronomy Journal, 80, 232-242.
Lim, P.O., Kim, H. J. e Nam, H. G. (2007). Leaf senescence. Annual Review of Plant Biology, 68, 115-136.
Machado, M., Gomes, E., Francisco, F., Bernert, A., Bespalhok Filho, J. e Deschamps, C. (2018). Micropropagation and Establishment of Humulus lupulus L. Plantlets under field conditions at southern Brazil. Journal of Agricultural Science, 10, 275-281.
Marcos, J. A. M., Nadal, J. L. O., Andión, J. P., Alonso, J. V., Pedreira-Ramisquido, J. M. G. e Paz, J. F. (2011). Guia del cultivo del lúpulo. Galícia.
Marschner, P. (2012). Marschner’s Mineral Nutrition of HigherPlants. Elsevier.
Mayer, L., Meneghini, J., Fior, C. S. e de Freitas, E. M. (2017). Progapagação de Passiflora caerulea L. por estaquia. Ilheringia – SérieBotânica, 72, 5-8.
Moraes, M. T. e Gusmão, A. G. (2021). How do water, compaction and heat stresses affect soybean root elongation? A review. Rhizosphere, 19, 100403.
Oliveira, M. V. R., Moreira, M. A. e Roters, D. F. (2019). Crescimento do lúpulo influenciado por diferentes níveis de acidez. VI Reunião Paranaense de ciência do solo.
Pagliarini, M. K., De Castilho, R. M. M., Moreira, E. R. e Alves, M. C. (2015). Caracterização física e química de substratos com diferentes proporções de resíduo de celulose. Ornamental Horticulture, 21, 33-38.
Paulus, D., Dall’Agnol, M., Becker, D. e Moura, C. A. (2020). Comprimento de estacas e doses de ácido indolbultirico na produção de mudas de lúpulo em hidroponia. VIII Congresso virtual de agronomia.
Pêgo, R. G., Vilela, C. e Fiorini, A. (2019). Propagation of Streptosolenjamesonii (Benth.) Miers by stem cutting treated with IBA in different substrates. Ornamental Horticulture, 25, 26–33.
Penã, M. L. P., Gubert, C., Tagliani, M. C., Bueno, P. M. C. e Biasi, L. A. (2012). Concentrações e formas de aplicação do ácido indolbutirico na propagação por estaquia dos mirtileiros cvs. Flórida e Clímax. Semina: Ciencias Agrarias, 33, 57-64.
Peragine, J. (2011). Growing your own hops, malts, and brewing herbs. Atlantic.
Peralta, M. A. M., Nava, J. R. G., Santos, G. G., García, A. R. R. e Salado, N. T. (2017). Reguladores del crecimento y substratosem la propagación vegetativa de nanche (Malpighiamexicana A. Juss. y Byrsonimacrassifolia (L) H. B. K.). Revista Brasileira de Fruticultura, 39, 1-9.
Rodrigues, M. A., Morais, J. S. e Castro, J. P. M. (2015). Jornada de lúpulo e cerveja: novas oportunidades de negócio. Instituto politécnico de Bragança.
Rosa, N. A. e Afonso, J. C. (2015). A química da cerveja. Química, 37, 98-105.
Sánchez, J. J. M., Hernández, J. J. V., Peralta, M. C. L. e Mata, J. J. (1998). Enraizado de estacas juveniles em cinco espécies de coníferas ornamentales: Effecto del ácido indolbutírico AIB Y de la temperatura. Revista Mexicana de Ciencias Forestales, 23, 29-38.
Sawicka, B., Spiewak, M., Kieltyka-Dadasiewicz, A., Skiba, D., Bienia, B., Krochmal-Marczal, B. e Pszczólkowski, P. (2021). Assessment of the Suitability of Aromatic and High-Bitter Hop Varieties (Humulus lupulus L.) for Beer Production in the Conditions of the Małopolska Vistula Gorge Region. Fermentation, 7, 104.
Silva, F. C., Eira, P. A., Raij, B. V., Silva, C. A., Abreu, C. A., Gianello, C., Pérez, D. V., Quaggio, J. Á., Tedesco, J. M., Abreu, M. F. e Barreto, W. O. (2009). Análises químicas para avaliação da fertilidade do solo. Em: F. C. Silva (Ed.). Manual de análises químicas de solos, plantas e fertilizantes. Embrapa.
Souza, A. F. F., Neto, E. C., Coelho Júnior, M. G., Nogueira, J. K. S. e Cordeiro, A. A. S. (2018). Efeito de diferentes concentrações de AIB na propagação por estaquia de Tabernaemontana Divaricata (L.). Agrarian Academy, 5, 204-211.
Sousa, M. J. A. C. (2005). Obtenção de Plantas de HumulusLupulus L. Resistentes a Vírus [Tese de doutorado]. Universidade de Lisboa.
Soil Survey Staff. (2014). Keys to Soil Taxonomy. Twelfth ed. USDA-Natural Resources Conservation Service.
Spósito, M. B., Ismael, R. V., Barbosa, C. M. A. e Tagliaferro, A. L. (2019). A cultura do lúpulo: Série produtor rural. Universidade de São Paulo.
Suttle, J. C. e Hultstrand, J. F. (1991). Ethylene-induced leaf abscission in cotton seedlings: The physiological bases for age-dependent differences in sensitivity. Plant physiology, 95, 29-31.
Taiz, L., Zeiger, E., Møller, I. M. e Murphy, A. (2017). Água e células vegetais. Em: L. Taiz (Ed.). Fisiologia e Desenvolvimento Vegetal. (pp. 83-98) 6ª edição.
Tedesco, M. J., Gianello, C., Bissani, C. A., Bohnen, H. e Volkweiss, S. J. (1995). Análise de solo plantas e outros materiais. Universidade Federal do Rio Grande do Sul.
Thomé, V. M. R., Zampieri, S., Braga, H. J., Pandolfo, C., Silva Junior, V. P., Bacic, I. L. Z., Laus Neto, J. A., Soldateli, D., Gebler, E. F., Dalle Ore, J. Á., Echeverria, L. C. R., Ramos, M. G., Cavalheiro, C. N. R., Deeke, M., Mattos, J. F. e Suski, P. P. (1999). Zoneamento agroecológico e socioeconômico da Santa Catarina. Epagri.
Wang, Z., Hong, X., Hu, K., Wang, X., Du, S., Li, Y., Hu, D., Cheng, K., An, B., e Li, Y. (2017). Impaired Magnesium Protoporphyrin IX Methyltransferase (CHlM) Impedes chlorophyll synthesis and plant growth in rice. Frontiers in Plant Science, 8, 1694.
Revista científica de la Asociación Argentina de la Ciencia del Suelo